Dr. Sergio A. V. Jannuzzi - Spektroskopie und Reaktivität von molekularen Katalysatoren
- Dr. Sergio Augusto Venturinelli Jannuzzi
- Projektleiter
- Spektroskopie und Reaktivität von molekularen Katalysatoren
- Anorganische Spektroskopie
- +49 (0)208 306 - 3586
- sergio.jannuzzi(at)cec.mpg.de
- Raum: 506
Vita
| B.Sc./M.Sc. | University of Campinas, BR (2005-2011) |
| Ph.D. | KU Leuven, BE, und University of Campinas, BR (2009-2011) |
| Postdoc | MPI CEC (2018 - 2020) |
| Gruppenleiter | MPI CEC (seit 2020) |
Awards
- Marie Skłodowska-Curie Actions Seal of Excellence, European Research Commission (2018)
- Lindau alumnus of the 67th Lindau Nobel Laureate Meeting, Lindau Nobel Laureate Meeting Council (2017)
- Selected participant of the Baden-Württemberg Post Conference Programme of the Lindau Nobel Laureate Meeting, Baden-Württemberg International (2017)
- NanoSystem Initiative Munich Research Award, LMU Munich (2010)
- Lavoisier Award of Best Student in Chemistry 2005-2009, Regional Council of Chemistry, 4th Region, Brazil (2009)
- II Assintecal/Petrobras Award in Adhesive Technology and Shoe Fastening Processes, Brazilian Association of Companies of Components for Leather, Footwear and Devices (2007)
Publications
Full publications list | ORCID
Selected MPI CEC publications
- Keilwerth, M., Mao, W., Venturinelli Jannuzzi, S. A., Grunwald, L., Heinemann, F. W., Scheurer, A., et al. (2023). From Divalent to Pentavalent Iron Imido Complexes and an Fe(V) Nitride via N-C Bond Cleavage. Journal of the American Chemical Society, (145), 873-887. doi:10.1021/jacs.2c09072.
- W. Mao, D. Fehn, F.W. Heinemann, A. Scheurer, M. van Gastel, S.A.Venturinelli Jannuzzi, S. DeBeer, D. Munz and K. Meyer. “Umpolung in a Pair of Cobalt(III) Terminal Imido/Imidyl Complexes”. Angewandte Chemie International Edition (2022) 61, e202206848. https://doi.org/10.1002/anie.202206848
- C Souilah, SAV Jannuzzi, D Demirbas, S Ivlev, M Swart, S DeBeer and A Casitas. “Synthesis of Fe(III) and Fe(IV) Cyanide Complexes Using Hypervalent Iodine Reagents as Cyano-Transfer One-Electron Oxidants”. Angewandte Chemie International Edition (2022), 61.22, e202201699. https://doi.org/10.1002/anie.202201699
- I Gerz, SAV Jannuzzi, KT Hylland, C Negri, DS Wragg, S Øien-Ødegaard, M Tilset, U Olsbye, S DeBeer and M Amedjkouh. “Structural Elucidation, Aggregation and Dynamic Behaviour of N,N,N,N-Copper(I) Schiff Base Complexes in Solid and in Solution: a Combined NMR, X-ray Spectroscopic and Crystallographic Investigation”. European Journal of Inorganic Chemistry (2021), 46, 4762–4775. https://doi.org/10.1002/ejic.20210072
Spektroskopie und Reaktivität von molekularen Katalysatoren

Zahlreiche Reaktionen, ohne die unser tägliches Leben undenkbar wäre, werden von molekularen Komplexen der Übergangsmetalle, die entweder natürlicher oder synthetischer Art sind, katalysiert. Zusätzlich zur Analyse von Edukten und Produkten erlaubt uns die Spektroskopie die Identifikation und Charakterisierung von aktiven Spezies, welche die beobachtete Reaktivität verursachen. Oft ist es nicht möglich aus einer spektroskopischen Beobachtung direkte Rückschlüsse auf die molekulare Struktur zu ziehen. Dies liegt unter anderem an den quantenmechanischen Auswahlregeln, welche für die Interaktion von elektromagnetischer Strahlung mit Materie gelten. Um diese Wissenslücke zu schließen, bedarf es molekularer Modellierung. Sie erlaubt es die experimentellen Daten dahingehend einzuordnen, dass eine elektronische Struktur vorgeschlagen werden kann und Einsichten in die erforschten chemischen Prozesse gewonnen werden können.
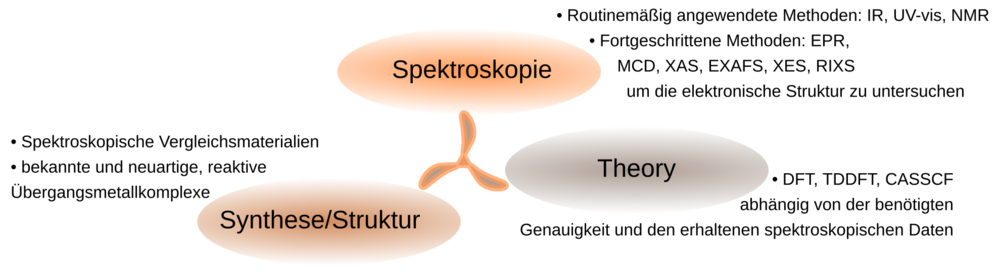
Um grundlegende Erkenntnisse über die Schlüsseleigenschaften zur Aktivierung von C-H-Bindungen durch Übergangsmetallkomplexen der 4. Periode zu erhalten, stützt sich die Arbeit unserer Gruppe auf drei Säulen: Synthese, Spektroskopie und molekulare Modellierung.
Während Enzyme die Synthese von synthetischen Katalysatoren inspirieren, erlaubt die Erforschung von biomimetischen Modellen ein besseres Verständnis der Struktur und Wirkmechanismuss des Enzyms dem es nachempfunden ist. Die Lytic polysaccharide monooxygenase1 (LPMO) weist ein lösungsmittelexponiertes aktives Zentrum mit einem einzelnen Kupferatom auf, welches in der Lage ist die C-H-Bindungen in unlöslichen Polysacchariden zu oxidieren. Dadurch wird das Polysaccharid in kleinere Teile zerlegt, die als erneuerbares Ausgangsmaterial für Fermentationen dienen können. Ob das Sauerstoffatom, welches das Enzym verwendet um das Substrat zu oxidieren, aus molekularem Sauerstoff oder Wasserstoffperoxid stammt, ist Gegenstand der aktuellen wissenschaftlichen Debatte.2 Die reaktiven Intermediate sowie der Mechanismus der Reaktion sind noch unerschlossen. Von besonderem Interesse sind Wechselwirkungen zwischen der ersten Koordinationssphäre um das Kupferatom und weiter entfernten Seitenketten in der zweiten Koordinationssphäre.
Referenzen
1. Vaaje-Kolstad, G.; Westereng, B.; Horn, S.J.; Liu, Z.; Zhai, H.; Sørlie, M.; Eijsink, V.G.; An oxidative enzyme boosting the enzymatic conversion of recalcitrant polysaccharides. Science 2010, 330(6001), 219-22.
2. Bissaro, B.; Røhr, Å.K.; Müller, G.; Chylenski, P.; Skaugen, M.; Forsberg, Z.; Horn, S.J.; Vaaje-Kolstad, G.; Eijsink, V.G.H.; Oxidative cleavage of polysaccharides by monocopper enzymes depends on H2O2. Nat Chem Biol. 2017, 13(10):1123-1128.


